|
||||
|
|
Интенсивный путь развития аграрной цивилизацииНовый взгляд на эволюцию. «Генетическая инженерия» в природных экосистемахСледует подчеркнуть принципиально важное обстоятельство: одно из важных положений современной генетики состоит в открытии способности наследственной системы к «естественной генетической инженерии». В клетке существует режим генетического поиска и реорганизации структуры и функции генома. Термин «вирус» этимологически обозначает «яд». Вплоть до 60-х годов XX века вирусы преимущественно рассматривались как болезнетворное начало. Но изучение вирусов многоклеточных организмов и бактерий (бактериофагов), открытие большого сходства мобильных генетических элементов с вирусами, а затем выявление повсеместного распространения вирусных последовательностей в геноме каждого изученного вида млекопитающих изменило представление о вирусах. Представление о повсеместности вирусов в биосфере, высказанное в середине 70-х годов (Жданов, Тихоненко, 1975), в настоящее время полностью подтверждено. Вирусы вездесущи. Может быть, именно поэтому их можно обнаружить при любом заболевании (у здоровых их, как правило, не ищут). У человека только в клетках кишечника число обнаруженных в норме и при патологии вирусов больше 120. К 1970-м годам стала ясна суть респираторных — «простудных» заболеваний, переносимых большинством горожан, которые являются отражением эпидемических вспышек размножения вирусов. Целенаправленное изучение путей распространения вирусов в природе привело в начале 80-х годов XX века к получению новой информации. Например, такие вирусы, как вирус полиомиелита, которые из-за своего видимого патогенного эффекта считались исключительно нейротропными, оказались обнаруженными в сточных водах и, стало быть, входят в группу энтеровирусов. Сточные воды оказались источником вспышки одной из форм вирусного гепатита, детского гастроэнтерита. Пути распространения вирусов в биоценозах, и соответственно, пути горизонтального межвидового переноса генетического материала, поразительны. Достаточно сказать, что РНК-содержащий вирус гриппа переносится водоплавающими перелетными птицами, но обнаружен и у китов и у планктонных организмов (Жданов, 1990). В эволюционном аспекте вирусы в природе являются самым мощным селективным фактором и самым мощным генератором наследственного полиморфизма, возникающего в результате популяционно-генетических взаимодействий типа паразит-хозяин. Другой важный фактор в эволюции — бактерии. Миллиарды лет бактерии были единственными обитателями биосферы. Ни человека, ни животных, ни высших растений не было на Земле, а бактерии уже были. Да они и сейчас настоящие «хозяева планеты». Бактерии — истинные космополиты: они завоевали толщи почв и все водные бассейны, они поселились и в нас самих. Они создавали и создают месторождения полезных ископаемых, они же превращают останки живых существ в материал для новой жизни, помогают нам переваривать пищу и готовить ее. Они способны и убивать нас, заразив болезнями. Биомасса этих мелких существ на много порядков превышает биомассу всех земных млекопитающих вместе с человеком. Горизонтальный перенос генов от одного организма в другой являлись существенным механизмом эволюции, в основном, у бактерий. Этот факт стал очевидным в последние несколько десятилетий. Джошуа Ледерберг в 1952 году ввел понятие «плазмида». Он обнаружил в кишечной палочке, кроме основной спиралевидной, вытянутой во весь свой немалый рост ДНК, еще и маленькие, свернутые в кольцо ДНК. О плазмидах заговорили медики, когда в 1959 году было доказано, что неэффективность многих антибиотиков обусловлена плазмидами, несущими гены устойчивости к антибиотикам. Плазмиды легко переходят от бактерии к бактерии, делая их невосприимчивыми к лекарствам. К примеру, вырабатываемый плазмидами фермент пенициллаза разрушает пенициллин, спасая бактерии от гибели. Что, конечно же, осложняет лечение больных. Детальные наблюдения характера возникновения опосредованной плазмидами устойчивости сделаны в Японии и Англии. В 1945 г. в Японии для борьбы с дифтерией стали применять сульфаниламид. Он был высокоэффективен только первые 5 лет. Вскоре появились устойчивые штаммы дифтерийной палочки, а уже некоторое время спустя 80-90% изолятов были устойчивыми. Затем сульфаниламид заменили антибиотиками. Но уже в 1952 г. от больного дифтерией был выделен штамм дифтерийной палочки, одновременно устойчивый к тетрациклину, стрептомицину и сульфаниламиду. А в 1964 г. половина всех бактериальных штаммов, выделенных из больных дифтерией, несла гены устойчивости одновременно к четырем антибиотикам. Эти гены устойчивости были собраны в одной плазмиде, способной распространяться среди бактерий горизонтально. Гены плазмид, в свою очередь, могут перекочевывать на хромосомы клеток-реципиентов. Считают, что таким путем в кишечную палочку попали гены, кодирующие ферменты инактивации антибиотиков. Возможно, эти гены впервые появились у почвенных бактерий, живущих рядом с грибами-продуцентами антибиотиков. В почвенных бактериях в геноме плазмид находятся детерминанты устойчивости к тяжелым металлам. Из природных резерватов плазмиды с транспозонами, несущие гены устойчивости, попадают к бактериям животных и человека и с помощью их распространяются по всему миру. То, что затрудняло работу медиков, пригодилось генным инженерам. А им нужны были переносчики реконструированных молекул ДНК в живые объекты. Правда, вначале на эту роль прочили вирусы-бактериофаги. Но, проникнув в клетку, вирус ведет себя как опасный хищник. Он переключает ресурсы клетки на удовлетворение своих нужд и примерно через полчаса губит ее. Иначе поступает плазмида — в отличие от вируса, она не убивает клетку-хозяйку. Плазмида и приютившая ее клетка осуществляют симбиоз. Плазмида защищает бактерию от, например, пенициллина. Клетка предоставляет плазмиде ресурсы для питания, размножения. Все эти особенности симбиоза бактерий и плазмид (особенно способность плазмид переходить «из рук в руки», от одной клетки к другой) оказались источниками генно-инженерных методов. Плазмидами Д. Ледерберг предложил обозначать все внеядерные генетические элементы, способные к автономной репликации. Сюда входят «каппа-частицы» у парамеций, экзогенные вирусы и т.д. Взгляд на плазмиды как на симбионты и альтернативный взгляд на них как на составную часть генома, согласно Д. Ледербергу, зависит от того, насколько широко исследователь трактует границы генома и наследственной системы организма. Именно особенности жизненных циклов вирусов, плазмид и бактерий привело в дальнейшем к созданию так называемых «векторов» — искусственно сконструированных молекул наследственности, которые могут переносить чужеродный материал от одного организма к другому. Какие генно-инженерные приемы подсмотрены в природеБлагодаря перемещающимся элементам, генофонды всех организмов потенциально составляют общий генофонд всего живого. Реализация этой потенции, т.е. передача генов между разными таксонами, детально документирована. У млекопитающих и птиц практически идентичные провирусные последовательности появились уже после их эволюционного обособления. Поток генов между далекими организмами является реальностью. Вопрос заключается только в том, насколько часто организмы присваивали чужеродные гены в качестве «благоприобретенных собственных функциональных генов». Наглядным примером горизонтального обмена между прокариотами и высшими эукариотами являются результаты исследований представленности в прокариотических геномах нуклеотидных последовательностей, типичных для эукариот (табл.1). Из этой таблицы следует, в частности, что в геноме симбионта человека, кишечной палочки, примерно 17% ДНК имеет эукариотическое происхождение. Хорошим примером естественной генетической трансформации является агробактериальная трансформация растительных клеток. Отличительная черта бактерий рода Agrobacterium (A.tumefaciens, A.rhizogenes) — способность вызывать развитие так называемых корончатых галлов (своего рода опухолей) у большого круга двудольных растений. При этом происходит перенос фрагмента ДНК агробактерии в геном растительных клеток. Такая клетка со встроенным участком агробактериальной ДНК продуцирует ряд органических веществ, служащих для агробактерии специфическими источниками углерода и азота. Такой перенос — уникальный природный процесс обмена генетической информацией между бактерией и растением, и именно его ученые взяли на вооружение для получения трансгенных растений, встраивая целевой ген в участок агробактериальной ДНК, переносимый в растение. Эффективность трансформации растительных клеток может быть увеличена за счет использования штаммов A.tumefaciens, обладающих повышенной вирулентностью по отношению к данному виду растений. Тем не менее, частота трансформации весьма низка — только одна из 10 тысяч растительных клеток становится носителем рекомбинантной ДНК. Возможно около 20 способов проникновения и межвидовой миграции генетических элементов, в их числе трансформация, трансдукция, перемещение транспозонов, плазмид, вирусов, неполовой обмен хромосомами и образование симбиотических ассоциаций. Информационная емкость переноса информации, выраженная в генах, варьирует от единиц до сотен и тысяч в случае плазмид и симбионтов. 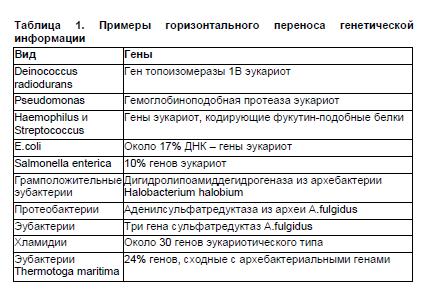 Под влиянием стресса резко увеличиваются частоты горизонтального обмена материалом наследственности между бактериями, у растений — частоты перекрестного опыления у самоопылителей. В последние годы в различных моделях стресса у многих видов высших организмов наблюдают увеличение частот рекомбинационных событий, транспозиций, различных мутационных событий. Отчетливые данные о связи дестабилизации генетического материала с действием стрессирующих факторов, полученнные Б. МакКлинток, впоследствии привели к развитию представлений о системах «природной генетической инженерии» (Shapiro. 1992,1995). Изначально термин «генетическая инженерия» применяли для обозначения целенаправленной манипуляции наследственными детерминантами с целью изменения существующих видов. В настоящее время этим термином обычно обозначают генетические манипуляции, с помощью которых формируется организм, имеющий новую комбинацию наследуемых признаков. Иначе ДНК-технологии можно определить как отрасль биологии, которая изучает явления и конструирование наследственности и изменчивости. Современный этап ДНК-технологий неразрывно связан с необходимостью увеличения источников благосостояния и здоровья человечества. ДНК-технологии стремительно увеличивают наши знания в одной из наименее исследованных областей — наследственности и законов ее изменения естественным и экспериментальным путем. Свыкшись с материальностью генов, человек, естественно, тут же захотел заняться генной хирургией. Для этого в природе имеются ферменты рестриктазы, с высокой точностью разрезающие молекулу ДНК в определенных сайтах (сочетаниях нуклеотидов), и ферменты лигазы, «сшивающие» такие разрывы. Именно эти ферменты послужили основой для создания строго запланированных генных конструкций. Использование рекомбинантных (перестроенных) ДНК различного происхождения составляет основу ДНК-технологий. Теоретически все 30-40 тысяч структурных генов человека и животных доступны теперь экспериментальному анализу. Поэтому желательна идентификация всех генов; составление карты тканеспецифичности их экспрессии; идентификация регуляторных областей генов; построение глобальной регуляторной карты генома; классификации генов по структурным и биохимическим функциям их продуктов; идентификация всех потенциальных белков и доменов; анализ распределения полиморфизма и мутаций; определение эволюционных и популяционных взаимосвязей; создание коллекции генетического материала и тд. Устойчивость нити ДНК в составе хромосом регулируется целой системой ферментов, контролирующих три матричных процесса — репликацию, транскрипцию и трансляцию, и три собственно генетических процесса — репарацию, рекомбинацию и сегрегацию нитей ДНК и хромосом. Белковые продукты «генов метаболизма ДНК» образуют комплексы, которые следят за устойчивостью нитей ДНК, надежностью их репликации и рекомбинации, корректируют однонитевые и двунитевые повреждения. Степень активности этих комплексов весьма чувствительна к физиологическому статусу клетки. Ю.Я. Керкис (1940) впервые показал, что спонтанные наследственные изменения возникают за счет нарушения внутриклеточного метаболизма и физиологического гомеостаза. Устойчивость ДНК и темп мутаций могут в случае клеточного стресса меняться в десятки и сотни раз. Началом эры генной инженерии растений принято считать 1973 год, когда впервые был проведен целенаправленный перенос гена. Фактически генная инженерия продолжает направление традиционной селекции сельскохозяйственных культур, однако достигает поставленных целей намного быстрее. Основные отличия генетической инженерии от традиционной селекции заключаются в том, что улучшение свойств культурных растений достигается либо улучшением существующей, либо созданием новой генетической вариации. При использовании традиционных методов скрещивания гарантия получения искомой комбинации генов, то есть желаемого признака у растения, практически отсутствует. Прогресс современной науки во многом определяется и в решающей степени зависит от экспериментальной и практической реализации новых идей и подходов в клеточной и молекулярной биологии. Химерные и трансгенные животные и растения — это наиболее яркое подтверждение потенциальных возможностей фундаментальной и прикладной науки. Такие организмы стали основными инструментами в исследованиях функций генов, процессов дифференцировки, эмбрионального развития, клеточной гибели и старения. Несомненный прорыв в деле создания химерных и трансгенных организмов связан с разработкой ЭСК-технологий и микрохирургической техники работы на изолированных зародышах. В этих технологиях эмбриональные стволовые клетки стали связующим звеном между системами in vitro и in vivo, что дало возможность легко переносить результаты исследования с клеточного уровня на уровень целого организма. При этом значительно повысилась эффективность метода трансгеноза — до 40-50% по сравнению с 1% при использовании техники инъекции чужеродной ДНК (генов) в пронуклеусы зародыша на стадии зиготы. ДНК-технологии позволяют исследовать и направленно изменять материал наследственности на разных уровнях его организации — генном, хромосомном, геномном, популяционно-генетическом. Интересно, что в смысле управления наследственностью «генетическую инженерию» использовали в течение тысячелетий безымянные селекционеры, благодаря которым еще в эпоху неолита и было введено в культуру абсолютное большинство возделываемых в настоящее время видов растений. Переходя непосредственно к описанию методов генетической трансформации, отметим, что на сегодняшний день молекулярная генетика располагает значительным набором знаний и приемов для осуществления переноса генов из одних организмов в другие. Технология создания трансгенных растений включает большое количество этапов, среди которых можно выделить: получение целевых генов, создание векторов; трансформацию растительных клеток; подтверждение трансформации молекулярно-биологическими методами — обнаружение функционирующего целевого гена; регенерация целого растения из трансформированных клеток. Подготовительный этап: конструирование вектора. На первом этапе конструирования рекомбинантной ДНК готовят вставки, пригодные для последующего соединения с вектором. В настоящее время наиболее часто используются 3 метода их получения: из фрагментов геномной ДНК; путем ферментативного или химического синтеза фрагментов ДНК; из сегментов ДНК, полученных с помощью ферментативного копирования РНК-матрицы in vitro. В качестве вектора, которым может быть любой небольшой внехромосомный элемент (плазмида, ДНК фага или вируса), для трансформации растительных клеток обычно используют бактериальные плазмиды. Следует отметить, что в большинстве случаев целевой ген подвергается модификации, поскольку, несмотря на универсальность генетического кода (он одинаков для всех организмов вне зависимости от уровня их организации), состав триплетов, кодирующих одни и те же аминокислоты у организмов, принадлежащих к разным видам, имеет некоторые отличия. Замена кодонов никоим образом не сказывается на первичной структуре белка, в то время как экспрессия гена может быть усилена в сотни раз. Необходимый уровень экспрессии целевого гена в клетках растения достигается посредством использования соответствующих регуляторных элементов, контролирующих работу гена, — промоторов и терминаторов. Следует отметить, что среди известных в настоящее время промоторов один из самых сильных — промотор 35S вируса мозаики цветной капусты, поэтому в большинстве случаев именно его используют в качестве регулятора экспрессии целевого гена. Таким образом, вносимая генетическая конструкция (вставка или кассета экспрессии) — это группа функционально связанных участков ДНК, состоящая из высокоактивного промотора, непосредственно за которым располагаются соответствующий целевой ген и терминатор транскрипции. После получения вектора и вставки начинается процесс конструирования рекомбинантной ДНК. Полученные молекулы ДНК вводят в бактериальные клетки для клонирования, что приводит к накоплению рекомбинантной ДНК. Эффективное увеличение количества ее копий возможно лишь при обеспечении оптимальных условий существования вектора, использующего метаболиты, ферменты и другие белки клетки-хозяина, а также ее аппарат белкового синтеза, поэтому основной инструмент молекулярного клонирования — совместимая комбинация хозяина и вектора. Наиболее широко применяются такие сочетания, когда в роли хозяина выступает штамм E.coli, а в роли вектора — его плазмида. Проникновение вектора в живые клетки E.coli проходит наиболее эффективно при условии повышенной проницаемости клеточных мембран, обусловленной, например, их локальным разрушением. Нарушение их целостности достигается либо воздействием электрического тока — электропорацией, либо посредством обработки клеток определенными химическими веществами, после чего перенос вектора происходит в течение нескольких минут. Векторы обычно содержат маркерные гены, благодаря которым осуществляется отбор клеток с измененным генотипом. Например, клетки, чувствительные к определенному антибиотику или токсину, можно использовать в комбинации с векторами, содержащими гены устойчивости к этим агентам. Выращивая микроорганизмы в условиях, при которых проявляется зависимость от маркерных генов, можно отобрать и размножить клетки, несущие требуемый генетический материал. Методология прикладного использования ДНК-технологийДНК-технология или генная (генетическая) инженерия — направление исследований в генетике, в рамках которого разрабатывают приемы, позволяющие по заранее намеченному плану перестраивать геном организмов (совокупность генетических элементов организма), изменяя в нем генетическую информацию. С помощью рестриктаз и лигаз получают перестроенные (химерные) молекулы ДНК. Их еще называют рекомбинантными — полученными в результате объединения in vitro в природе никогда вместе не существующих фрагментов ДНК (например, ДНК бактерии и растения). Живую систему для размножения рекомбинантных молекул выбирают среди бактерий. Получение рекомбинантных ДНК в количестве, необходимом для проведения генетической модификации, позволяет перейти непосредственно к ключевому этапу получения ГМ культур: трансформации растительных клеток. В идеале трансформационная система должна отвечать определенным условиям: быть простой, эффективной и дешевой. Однако, несмотря на сравнительно широкий выбор методических приемов, всем требованиям не соответствует ни один из них. Тем не менее в настоящее время для производства трансгенных культур в промышленных масштабах в основном применяются два способа модификации растительного генома — агробактериальный (то, как это делается в природе, см. выше) и баллистический, баллистическая трансформация растительных клеток (еще называемый микробомбардировкой, методом ускорения частиц, биолистикой — термин, произошедший от объединения слов «биология» и «баллистика») состоит в «обстреле» растительных клеток золотыми или вольфрамовыми частицами, которые играют роль переносчика рекомбинантной ДНК. В сущности, микрочастицы могут быть из любого химически инертного металла с достаточно высокой молекулярной массой (золото, вольфрам, палладий, родий, платина, индий), чтобы не образовывать с ДНК металлорганических комплексов и обладать достаточно высокой кинетической энергией для эффективной пенетрации клеточной стенки. Частицам размером 1,5-3 микрона, конъюгированным с ДНК, придается скорость 300-600 м/сек посредством электрического разряда или декомпрессии в направлении клеток-мишеней, подлежащих трансформации. Несмотря на то, что эффективность этого способа невысока (не более 15%), баллистический метод — весьма распространенный прием трансформации однодольных растений. В последнее время разработан и успешно применен комбинированный метод трансформации, названный агролистическим. Он основан на объединении баллистического и агробактериального способов и заключается во введении в геном растения каким-либо физическим методом (в большинстве случаев баллистическим) чужеродной ДНК, включающей агробактериальные гены. Конечный этап — получение трансгенных растений, как правило, преодолевается легче, чем предыдущие процедуры. Благодаря тому, что многие клетки растений тотипотентны, то есть из любой единичной клетки может вырасти целое плодоносящее растение, трансгенные растения получают из трансформированных клеток. Культивирование растений с модифицированным геномом включает несколько серий пересевов на селективных средах. Длительность регенерации трансформированных растений достигает нескольких месяцев, причем все это время они находятся в среде с высокими концентрациями селективных веществ. Как правило, применяются маркерные гены двух основных типов — селективные и репортерные. Селективные придают растениям устойчивость к антибиотикам или гербицидам, позволяя трансформированным растениям расти в условиях действия селективных агентов. Репортерные гены детерминируют синтез нейтральных для клеток белков, наличие которых в тканях может быть легко установлено. При получении генетически модифицированного растения, устойчивого к пестицидам, ген устойчивости выступает как в роли целевого, так и селективного гена. Присутствие маркерных генов, особенно устойчивых к антибиотикам, служит одним из главных доводов против использования трансгенных продуктов. Потому-то и был разработан и теперь активно применяется ряд методических подходов, обеспечивающих элиминацию маркерного гена, когда фактически он уже не нужен. После получения целого трансгенного растения проводится анализ геномной ДНК растений, направленный на то, чтобы определить присутствие целевого гена. Он проводится различными путями. В большинстве случаев это достаточно сложные и дорогостоящие лабораторные методы, например, ПЦР-анализ, рестрикционный анализ и др. Заключительная стадия лабораторного тестирования ГМ растений включает биологические исследования, направленные на подтверждение стабильного фенотипического проявления целевого признака. С использованием описанных выше подходов к настоящему времени в мире созданы и доведены до испытаний в полевых условиях ГМ формы сельскохозяйственных растений, относящиеся более чем к 50 видам. Так, получены трансгенные формы томатов (более 260), сои (более 200), хлопчатника (более 150), тыквенных растений (более 80), табака (более 80), а также пшеницы, риса, подсолнечника, огурцов, салата, яблонь и других (более 70). Из них значительную часть представляют растения, устойчивые к насекомым-вредителям и гербицидам. Большинство производящихся в настоящее время в промышленных объемах ГМ сельскохозяйственных растений (или растений первого поколения) имеют свойства, обеспечивающие повышение урожайности или облегчение уборки, хранения, переработки урожая. Эти качества позволяют снизить применение гербицидов и инсектицидов, что оказывает положительное влияние на окружающую среду, сократить количество технологических операций при переработке, а также уменьшить потери урожая, повысить качество продукции, сэкономить средства и материальные ресурсы. |
|
||
|
Главная | В избранное | Наш E-MAIL | Добавить материал | Нашёл ошибку | Наверх |
||||
|
|
||||
